工程化肝组织在动物体内按需可控生长,为开发智能实体器官疗法奠定基础
发表于最新《科学进展》的研究报告提出了一种有望革新肝脏疾病治疗的突破性技术。由美国哈佛大学怀斯生物启发工程研究所、波士顿大学及麻省理工学院共同开发的“BOOST”策略,成功在小鼠体内实现了工程化肝组织的按需、可控生长。这项技术为未来开发智能的实体器官疗法,应对供体器官严重短缺困境,奠定了关键基础。
末期肝病患者常因肝脏损伤过重而无法修复,只能选择肝移植,但需求远大于供给。尽管科学家长期致力于在实验室中构建完整的移植肝脏,但如何让这些组织长到足够大且具备功能,始终是巨大挑战。
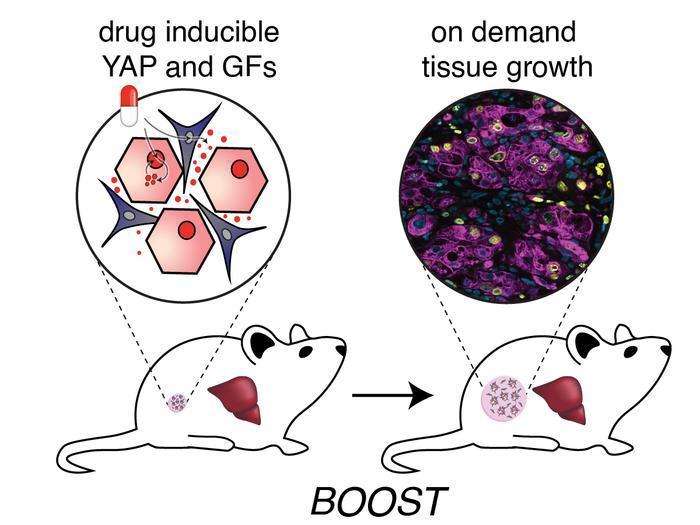
团队的设想是先行植入一个微型肝脏雏形,再于植入后引导它在患者体内安全地生长壮大。此项名为“通过合成生物学触发的按需生物工程生长”(BOOST)的研究,正是该理念的实践。
团队确定了一组4种生长因子的组合,能有效诱导培养皿中的人原代肝细胞增殖。为使这一过程在活体内安全、可控,团队改造了成纤维细胞,使其能分别分泌这4种关键生长因子,同时让肝细胞表达稳定。更重要的是,所有这些外源基因的表达都设计为“诱导型”,即其开启完全依赖于一种常见且安全的药物——多西环素。一旦停止给药,基因表达随之关闭,生长信号即告中断。
体外实验证实,经过连续7天的多西环素刺激,这些微型肝组织体积显著增大;撤去药物后,细胞增殖便停止。随后的小鼠体内实验取得了更令人鼓舞的结果,团队将工程化的微型肝组织植入健康小鼠体内,用多西环素诱导。7天后,植入组织中的工程化肝细胞数量增长了约5倍,并且组织内部实现了血管化,以满足其生长带来的代谢需求。整个过程小鼠耐受良好,未出现明显的免疫排斥或肿瘤样增生。
这一结果意义重大,BOOST策略首次在完全健康的宿主体内,实现了对植入肝组织生长的远程、按需控制。同时,这种智能化“按需生长”的理念,对于同样面临规模化挑战的心脏、胰腺等工程组织治疗领域,也具有广泛的启发意义。















